وجود فلزات سنگین در آب و پساب های صنعتی یکی از مهم ترین مشکلات زیست محیطی در جهان امروز است. در میان این فلزات، مس (Cu) جایگاه ویژه ای دارد، زیرا اگرچه عنصری ضروری برای بدن انسان و گیاهان است، اما در غلظت های بالا می تواند به شدت سمی و خطرناک باشد. ورود مس به منابع آبی معمولاً از طریق پساب صنایع فلزکاری، آبکاری، ذوب فلزات و استخراج معادن صورت می گیرد.
تجمع مس در بدن آبزیان می تواند به اختلالات فیزیولوژیکی، مرگ و کاهش تنوع زیستی منجر شود. از سوی دیگر، مصرف آب آشامیدنی آلوده به مس باعث آسیب به کبد و کلیه، تهوع و مشکلات گوارشی می شود. بنابراین حذف مس از آب و فاضلاب، گامی اساسی در حفاظت از محیط زیست و سلامت عمومی است. در این مقاله، به صورت جامع و کاربردی به معرفی روش های مختلف حذف مس از آب و پساب ها پرداخته می شود و مزایا، معایب و کاربرد هر روش بررسی خواهد شد.
منابع اصلی آلودگی مس در آب و فاضلاب
مس به عنوان یکی از پرکاربردترین فلزات صنعتی، در صنایع مختلفی مورد استفاده قرار می گیرد. در نتیجه، آلودگی های ناشی از این فلز معمولاً در نقاط صنعتی و شهری مشاهده می شود. برخی از مهم ترین منابع آلودگی مس عبارتند از:
- صنایع آبکاری و فلزکاری: در فرآیندهای پوشش دهی فلزی، محلول های حاوی یون مس وارد پساب می شوند.
- معادن استخراج و ذوب مس: پساب ناشی از شست وشوی سنگ معدن و باطله ها دارای غلظت بالای مس است.
- صنایع الکترونیک و تولید باتری: استفاده از مس در مدارها و آلیاژها باعث آلودگی آب های شست وشو می شود.
- کارخانه های تولید لوله و کابل مسی
بر اساس استاندارد سازمان جهانی بهداشت (WHO)، حد مجاز مس در آب آشامیدنی 2 میلی گرم در لیتر است. در حالی که در بسیاری از پساب های صنعتی، این مقدار تا ده ها برابر بیشتر گزارش شده است. بنابراین تصفیه مؤثر چنین پساب هایی از نظر قانونی و زیست محیطی ضروری است.

خطرات وجود مس در آب و فاضلاب
مس یکی از فلزات سنگین و ضروری برای بدن انسان، حیوانات و گیاهان است، اما تنها در مقادیر بسیار کم (در حد میکروگرم بر لیتر) مفید است. هنگامی که غلظت مس در آب از حد مجاز فراتر رود، به یک آلاینده خطرناک و سمی تبدیل می شود که می تواند سلامت انسان و محیط زیست را به شدت تهدید کند. در ادامه، اثرات و خطرات وجود مقادیر زیاد مس در آب از جنبه های مختلف بررسی می شود.
اثرات مس بر سلامت انسان
مقدار مجاز مس در آب آشامیدنی بر اساس استاندارد سازمان جهانی بهداشت حدود 2 میلی گرم در لیتر است. غلظت های بالاتر از این مقدار می تواند موجب بروز مشکلات متعددی در بدن شود.
- مشکلات گوارشی: مصرف آب حاوی مس بیش از حد مجاز باعث بروز علائمی مانند تهوع، استفراغ، دل درد، اسهال و احساس طعم فلزی در دهان می شود. این علائم در افرادی که دستگاه گوارش حساس تری دارند (مانند کودکان و سالمندان) شدیدتر است.
- آسیب به کبد و کلیه ها: در صورت مصرف طولانی مدت آب آلوده به مس، یون های مس در بافت های بدن تجمع پیدا می کنند. این تجمع می تواند باعث التهاب کبد، نارسایی کلیوی و تخریب سلول های کبدی شود. بیماری های مرتبط با تجمع مس مانند بیماری ویلسون از نمونه های شناخته شده این اثرات هستند.
- اثرات عصبی: غلظت بالای مس در خون ممکن است باعث اختلال در سیستم عصبی مرکزی شود و علائمی مانند سردرد، بی قراری، افسردگی، کاهش تمرکز و خستگی مزمن ایجاد کند.
- اثرات بر سیستم ایمنی و هموگلوبین: مصرف مداوم آب حاوی مس زیاد ممکن است منجر به کاهش جذب آهن و روی در بدن شود و در نتیجه کم خونی، ضعف سیستم ایمنی و اختلال در عملکرد آنزیم ها را به دنبال داشته باشد.
- خطر برای نوزادان: نوزادان و کودکان خردسال به دلیل نارس بودن سیستم متابولیکی، حساسیت بسیار بالایی به مس دارند. مصرف آب آلوده می تواند باعث آسیب کبدی و عصبی دائمی در آنان شود.
اثرات مس بر حیات آبزیان
مس در غلظت های پایین برای برخی از موجودات آبزی ضروری است، اما در غلظت های بالاتر از چند میکروگرم بر لیتر به شدت سمی می شود.
- یون های مس می توانند تنفس آبزیان را مختل کنند، زیرا به آبشش ها آسیب می زنند و انتقال اکسیژن را کاهش می دهند.
- تجمع مس در بدن ماهی ها باعث اختلال در سیستم عصبی، کاهش رشد، و ناتوانی در تولیدمثل می شود.
- در غلظت های بالا، مس می تواند مرگ سریع پلانکتون ها، جلبک ها و بی مهرگان آبزی را به دنبال داشته باشد، که این امر تعادل اکولوژیکی آب را به هم می زند.
در فاضلاب های صنعتی، غلظت مس معمولاً چندین برابر حد مجاز برای آبزیان است و در صورت تخلیه مستقیم به رودخانه ها، می تواند اکوسیستم های آبی را به طور کامل نابود کند.
اثرات مس بر گیاهان و خاک
وجود مس در آب آبیاری یا فاضلاب های صنعتی که برای کشاورزی استفاده می شوند، می تواند برای گیاهان مضر باشد.
- تجمع یون های مس در خاک باعث کاهش جذب عناصر ضروری مانند آهن، روی و منگنز می شود و در نتیجه رشد گیاه را کند می کند.
- مس زیاد موجب زردی برگ ها، کاهش فتوسنتز و کاهش عملکرد محصول می شود.
- در خاک های اسیدی، تحرک مس بیشتر است و به راحتی توسط ریشه جذب می شود که این امر خطر سمیت گیاهی را افزایش می دهد.
- از آنجا که فلز مس در محیط تجزیه ناپذیر است، در درازمدت موجب آلودگی دائمی خاک های کشاورزی می شود.
اثرات زیست محیطی و اکولوژیکی
آلودگی آب با مس نه تنها برای انسان و موجودات زنده خطرناک است، بلکه تعادل اکولوژیکی محیط زیست را نیز مختل می کند.
- مس در محیط های آبی می تواند با مواد آلی و معدنی ترکیب شده و در رسوبات ته نشین شود. این رسوبات به مرور به منبع ثانویه آلودگی تبدیل می شوند.
- در طول زمان، تغییر شرایط فیزیکی یا شیمیایی آب (مثل تغییر pH یا دما) ممکن است باعث آزادسازی مجدد مس از رسوبات و ورود دوباره آن به زنجیره غذایی شود.
- مس به عنوان یک بیوساید (عامل ضد میکروب) شناخته می شود و می تواند جمعیت باکتری های مفید در محیط را کاهش دهد؛ در نتیجه فرآیندهای طبیعی تصفیه بیولوژیکی در آب و خاک دچار اختلال می شوند.

انواع روش های حذف مس از آب و فاضلاب
در حال حاضر، روش های گوناگونی برای حذف مس از آب و فاضلاب وجود دارد که می توان آنها را در سه گروه اصلی فیزیکی، شیمیایی و بیولوژیکی طبقه بندی کرد. انتخاب روش مناسب بستگی به غلظت مس، نوع پساب، هزینه و اهداف تصفیه دارد.
روش های فیزیکی حذف مس از آب و فاضلاب
روش های فیزیکی در تصفیه آب و فاضلاب به مجموعه ای از فرآیندها گفته می شود که در آن ها، آلودگی ها بدون انجام واکنش شیمیایی و تنها بر اساس ویژگی های فیزیکی مانند اندازه ذرات، تخلخل، یا جذب سطحی جداسازی می شوند. این روش ها معمولاً به دلیل سادگی، هزینه پایین و راندمان قابل قبول، در صنایع مختلف برای حذف فلزات سنگین از جمله مس بسیار پرکاربرد هستند. در ادامه، مهم ترین روش های فیزیکی حذف مس از آب و فاضلاب به صورت تفصیلی معرفی می شوند.
جذب سطحی
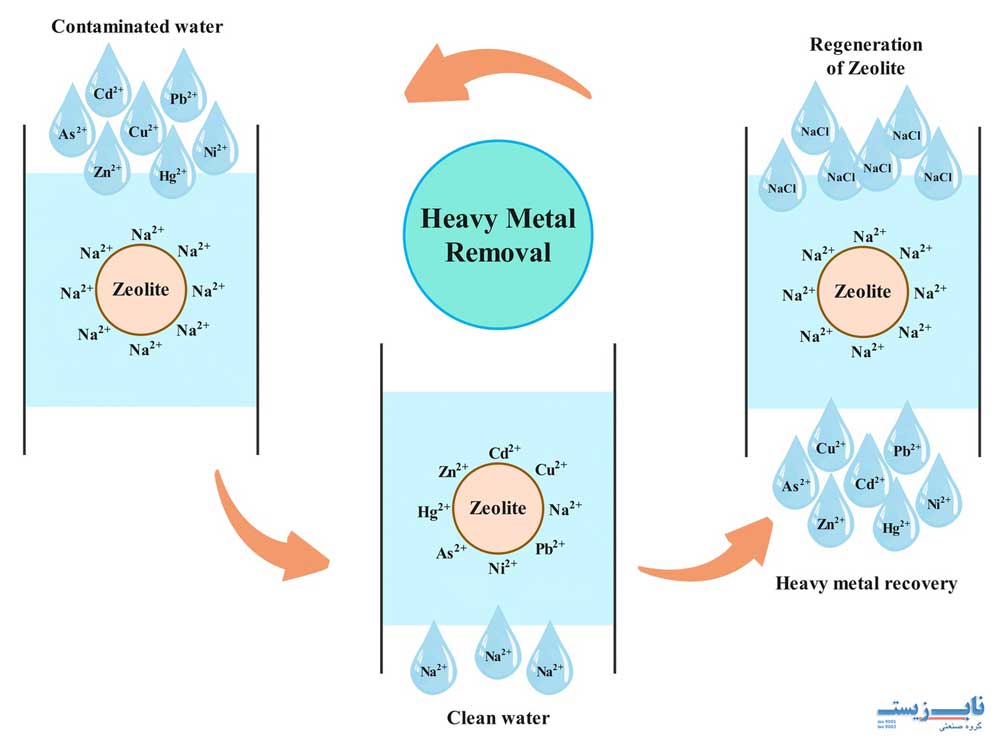
فرآیند جذب سطحی یکی از مؤثرترین روش های فیزیکی برای حذف یون های فلزی از آب است. در این روش، یون های مس محلول در آب به سطح مواد جامد جاذب متصل می شوند. این اتصال می تواند از طریق نیروهای فیزیکی مانند واندروالس یا پیوندهای ضعیف یونی انجام گیرد. مواد جاذب مورد استفاده در این فرآیند شامل کربن فعال، زئولیت، خاک رس، بیوچار، سیلیکا ژل و نانوذرات اکسید فلزی مانند اکسید آهن و منگنز هستند.
این روش به دلیل کارایی بالا و هزینه نسبتاً پایین، یکی از محبوب ترین روش ها در تصفیه پساب های صنعتی حاوی مس است. جاذب ها پس از اشباع شدن قابل احیا و استفاده مجدد هستند، هرچند فرآیند احیا ممکن است موجب افت نسبی ظرفیت جذب شود. بازده حذف مس در این روش معمولاً بین 80 تا 95 درصد گزارش شده است. جذب سطحی به ویژه برای پساب های با غلظت متوسط مس کاربرد دارد و در تصفیه خانه های صنایع آبکاری، مدار چاپی و فلزکاری بسیار مورد استفاده قرار می گیرد.
تبادل یونی
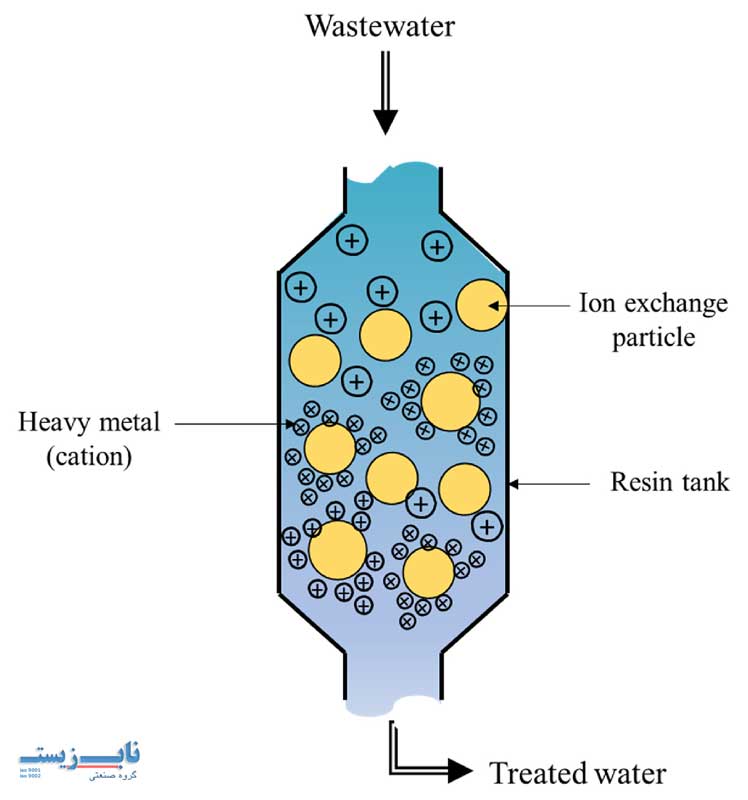
روش تبادل یونی مبتنی بر جایگزینی یون های مس محلول در آب با یون های موجود در رزین تبادل یونی است. رزین های مورد استفاده معمولاً از پلیمرهایی با گروه های عاملی فعال ساخته می شوند که قابلیت تبادل یون های مثبت (کاتیونی) یا منفی (آنیونی) را دارند. برای حذف مس، رزین های کاتیونی قوی مانند رزین های سولفوناته کاربرد بیشتری دارند.
در این فرآیند، هنگامی که آب آلوده از بستر رزینی دستگاه سختی گیر عبور می کند، یون های مس (Cu²⁺) به جای یون های سدیم (Na⁺) یا هیدروژن (H⁺) در سطح رزین جایگزین می شوند. پس از اشباع رزین، با عبور محلول های اسیدی یا نمکی می توان آن را احیا کرد و مجدداً مورد استفاده قرار داد.
مزیت مهم تبادل یونی، دقت بسیار بالای آن در حذف فلزات حتی در غلظت های پایین است. با این حال، هزینه بالای رزین ها و حساسیت سیستم به وجود ذرات معلق یا روغن در فاضلاب از محدودیت های این روش به شمار می رود. روش تبادل یونی بیشتر در تصفیه آب آشامیدنی، آب بویلرها و فاضلاب هایی با غلظت کم فلزات سنگین به کار می رود.
فیلتراسیون و میکروفیلتراسیون
فیلتراسیون یکی از ساده ترین و قدیمی ترین روش های فیزیکی تصفیه است که در آن، مواد معلق و ذرات جامد از طریق فیلترهای متخلخل از آب جدا می شوند. در مورد حذف مس، این روش معمولاً برای جداسازی رسوبات یا ذرات حاوی ترکیبات مسی به کار می رود، نه برای حذف یون های محلول.
در سیستم های صنعتی، فیلتر شنی، فیلتر کربنی و کارتریجی بیشترین کاربرد را دارند. برای ذرات کوچک تر، از غشاهای میکروفیلتراسیون با اندازه منافذ بین 0.1 تا 1 میکرومتر استفاده می شود. فیلتراسیون معمولاً به عنوان مرحله پیش تصفیه پیش از فرآیندهای دقیق تر مانند اسمز معکوس یا تبادل یونی استفاده می شود تا از گرفتگی غشاها و افت فشار جلوگیری شود. مزیت اصلی این روش، سادگی، هزینه پایین و سهولت در بهره برداری است. اما از آنجا که قادر به حذف یون های محلول مس نیست، به تنهایی برای تصفیه کامل فاضلاب های فلزی کافی نخواهد بود.
اسمز معکوس
اسمز معکوس یکی از پیشرفته ترین روش های فیزیکی برای حذف یون های فلزی محلول، از جمله یون های مس است. در این فرآیند، آب آلوده تحت فشار زیاد (5 تا 20 بار) از میان غشای نیمه تراوا عبور داده می شود. مولکول های آب از فیلتر ممبران عبور می کنند، در حالی که یون های فلزی و سایر ناخالصی ها پشت غشا باقی می مانند. غشاهای مورد استفاده معمولاً از پلی آمید یا سلولز استات ساخته می شوند و توانایی بالایی در حذف ذرات، نمک ها و فلزات سنگین دارند.
راندمان حذف مس در دستگاه آب شیرین کن صنعتی با روش اسمز معکوس بیش از 95 درصد است. از جمله مزایای این روش می توان به تولید آب با خلوص بالا، حذف هم زمان چندین نوع آلاینده و عدم نیاز به مواد شیمیایی اشاره کرد. در مقابل، هزینه اولیه بالا، نیاز به فشار زیاد و گرفتگی دوره ای غشا از چالش های این سیستم است. اسمز معکوس در صنایع دارویی، غذایی، الکترونیک و تصفیه نهایی پساب های صنعتی کاربرد فراوان دارد.
نانوفیلتراسیون
نانوفیلتراسیون فرآیندی مشابه اسمز معکوس است اما منافذ غشای آن کمی بزرگ تر (در حدود 1 تا 10 نانومتر) است. این ویژگی باعث می شود که یون های دوظرفیتی مانند یون مس (Cu²⁺) به خوبی حذف شوند، در حالی که برخی از یون های تک ظرفیتی مانند سدیم ممکن است از غشا عبور کنند.
این روش مصرف انرژی کمتری نسبت به اسمز معکوس دارد و درعین حال بازده بالایی برای حذف فلزات سنگین ارائه می دهد. نانوفیلتراسیون به ویژه برای بازیافت آب و حذف آلاینده های آلی و معدنی هم زمان مورد استفاده قرار می گیرد. از مزایای آن می توان به هزینه متوسط، مصرف انرژی کمتر و راندمان بالا اشاره کرد، اما همانند سایر سیستم های غشایی، گرفتگی و حساسیت به تغییر pH از چالش های آن است.

روش های شیمیایی حذف مس از آب و فاضلاب
روش های شیمیایی از مؤثرترین و پرکاربردترین فناوری ها برای حذف فلزات سنگین از آب و فاضلاب به شمار می روند. در این روش ها، از واکنش های شیمیایی برای تبدیل یون های محلول فلز به ترکیبات نامحلول، قابل ته نشینی یا جداسازی استفاده می شود. این دسته از روش ها معمولاً در تصفیه پساب های صنعتی حاوی فلزات مانند مس، روی، نیکل، کروم و سرب به کار می روند. در ادامه، مهم ترین روش های شیمیایی حذف مس از آب و فاضلاب معرفی و تشریح شده اند.
رسوب گذاری شیمیایی
رسوب گذاری شیمیایی رایج ترین و ساده ترین روش شیمیایی برای حذف یون های مس از فاضلاب است. در این فرآیند، با افزودن مواد قلیایی مانند آهک (Ca(OH)₂)، سود سوزآور (NaOH) یا کربنات سدیم (Na₂CO₃)، pH محلول افزایش می یابد و یون های مس (Cu²⁺) به شکل ترکیبات نامحلول مانند هیدروکسید مس (Cu(OH)₂) یا کربنات مس (CuCO₃) رسوب می کنند.
این رسوبات جامد به صورت لجن ته نشین می شوند و سپس از طریق ته نشینی، فیلتراسیون یا سانتریفیوژ جدا می گردند. بازده حذف مس در این روش معمولاً بین 90 تا 99 درصد است. مزیت اصلی این روش، سادگی و هزینه پایین مواد شیمیایی است. با این حال، تولید حجم قابل توجهی لجن و نیاز به دفع مناسب آن از چالش های اصلی محسوب می شود. برای بهبود راندمان، اغلب از ترکیبات کمکی مانند پلی الکترولیت ها جهت تسریع ته نشینی استفاده می شود.
اکسیداسیون و احیا
در روش های اکسیداسیون و احیا، از واکنش های شیمیایی برای تغییر حالت اکسیداسیون فلزات و تبدیل آن ها به فرم های قابل جداسازی استفاده می شود. در مورد مس، هدف اصلی کاهش یون های مس از حالت دوظرفیتی (Cu²⁺) به حالت فلزی (Cu⁰) یا ترکیبات نامحلول است.
به عنوان مثال، با افزودن عوامل کاهنده ای مانند سولفیت سدیم (Na₂SO₃)، هیدرازین (N₂H₄) یا آهن صفر ظرفیتی (Fe⁰) می توان یون های مس را به مس فلزی کاهش داد که به صورت ذرات جامد ته نشین می شود. در مقابل، در برخی شرایط ممکن است از مواد اکسیدکننده مانند پرمنگنات پتاسیم (KMnO₄) یا کلر (Cl₂) برای تبدیل ترکیبات آلی مس به فرم های معدنی قابل رسوب استفاده شود. این روش معمولاً برای تصفیه فاضلاب های با غلظت بالا یا پساب هایی که حاوی ترکیبات پیچیده مس هستند، به کار می رود. مزیت آن، امکان بازیافت فلز مس از لجن تولیدی است.
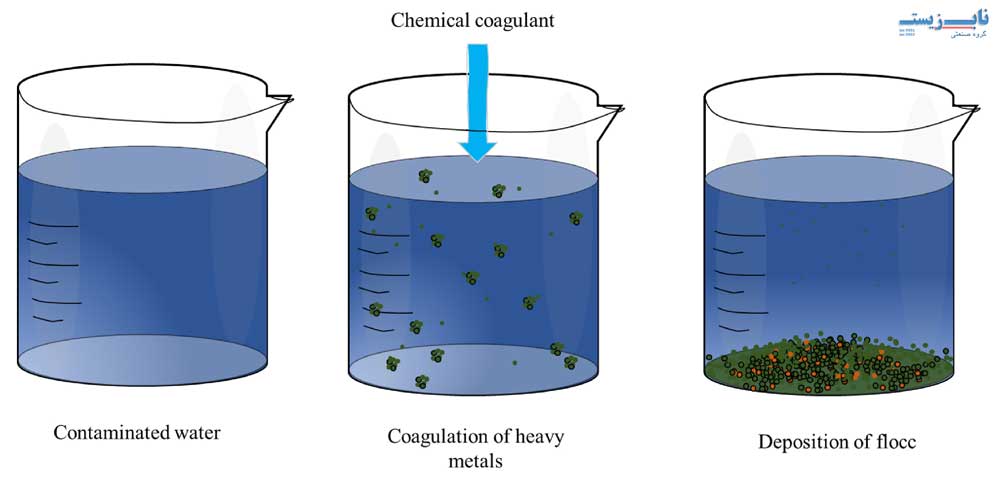
انعقاد و لخته سازی
انعقاد و لخته سازی یکی دیگر از روش های شیمیایی مهم در حذف مس از آب و فاضلاب است که معمولاً همراه با رسوب گذاری انجام می شود. در این فرآیند، با افزودن مواد منعقدکننده مانند سولفات آلومینیوم (Al₂(SO₄)₃)، کلرید آهن (FeCl₃) یا پلی کلراید آلومینیوم (PAC)، ذرات ریز و کلوئیدی حاوی مس به یکدیگر متصل شده و توده های بزرگ تری موسوم به «لخته» تشکیل می دهند.
این لخته ها به دلیل افزایش وزن به راحتی ته نشین می شوند و از فاضلاب جدا می گردند. برای بهبود راندمان، معمولاً پس از مرحله انعقاد، مواد پلیمری کمک منعقدکننده (مانند پلی الکترولیت ها) نیز به سیستم اضافه می شود. این روش به ویژه زمانی مؤثر است که مس به صورت ذرات معلق یا کمپلکس های کلوئیدی در آب وجود داشته باشد. ترکیب آن با رسوب گذاری باعث کاهش چشمگیر غلظت مس در پساب خروجی می شود.
ترسیب با سولفیدها
ترسیب با سولفیدها یکی از کارآمدترین روش ها برای حذف فلزات سنگین از جمله مس از فاضلاب است. در این روش، ترکیبات حاوی سولفید مانند سولفید سدیم (Na₂S)، سولفید هیدروژن (H₂S) یا تیو سولفات ها به فاضلاب اضافه می شوند. یون های سولفید با یون های مس واکنش داده و سولفید مس (CuS) نامحلول را تشکیل می دهند. این رسوب از نظر پایداری شیمیایی بسیار مقاوم است و در محدوده گسترده ای از pH نامحلول باقی می ماند.
در نتیجه، این روش حتی در فاضلاب های پیچیده با ترکیبات شیمیایی متنوع، راندمان بالایی (تا 99٪) دارد. مزیت دیگر این روش، حجم بسیار کم لجن تولیدی و پایداری زیاد آن در برابر انحلال مجدد است. با این حال، بوی نامطبوع گاز H₂S و خطرات زیست محیطی در صورت کنترل نامناسب، از چالش های اجرایی آن محسوب می شود.
استخراج شیمیایی یا استخراج حلالی
در این روش، از حلال های آلی برای انتقال یون های مس از فاز آبی (آب یا فاضلاب) به فاز آلی استفاده می شود. ترکیبات آلی مانند اکسی یمین ها (مثل LIX 984) و کربوکسیلیک اسیدها از جمله حلال های معمول در این فرآیند هستند. پس از انتقال یون های مس به فاز آلی، با تغییر pH یا افزودن اسید می توان مس را دوباره استخراج و بازیابی کرد.
به همین دلیل، این روش بیشتر در سیستم هایی به کار می رود که هدف علاوه بر تصفیه، بازیافت اقتصادی مس نیز باشد؛ مانند صنایع آبکاری و فرآوری سنگ معدن مس. استخراج شیمیایی دقت بالایی دارد، اما هزینه تجهیزات و مواد شیمیایی در آن نسبتاً زیاد است و معمولاً برای مقادیر کم یا فاضلاب های خاص به صرفه است.
خنثی سازی و تنظیم pH
تنظیم pH یک مرحله کلیدی در تقریباً تمام فرآیندهای شیمیایی حذف مس محسوب می شود. از آنجا که انحلال و رسوب فلزات به شدت به pH بستگی دارد، با کنترل دقیق این پارامتر می توان شرایط بهینه برای حذف مس را فراهم کرد. به عنوان مثال، در pH بین 8 تا 10، هیدروکسید مس بیشترین پایداری را دارد و راندمان رسوب گذاری در این محدوده بسیار بالا است. بنابراین، پیش از انجام هر فرآیند شیمیایی، معمولاً با استفاده از آهک یا سود، pH تنظیم می شود.
روش های بیولوژیکی حذف مس از آب و فاضلاب
روش های بیولوژیکی بر پایه استفاده از میکروارگانیسم ها (باکتری ها، جلبک ها، قارچ ها و گیاهان) برای حذف، جذب یا تبدیل آلاینده ها در آب و فاضلاب عمل می کنند. این روش ها به دلیل سازگاری با محیط زیست، هزینه پایین و تولید لجن کمتر نسبت به روش های شیمیایی و فیزیکی، در سال های اخیر مورد توجه ویژه قرار گرفته اند. در زمینه حذف فلز مس، موجودات زنده می توانند از طریق جذب سطحی، جذب درون سلولی، ترسیب زیستی یا تغییر شیمیایی فلز، آن را از محیط حذف کنند. در ادامه، مهم ترین روش های بیولوژیکی حذف مس از آب و فاضلاب توضیح داده می شوند.
حذف زیستی از طریق میکروارگانیسم ها
بسیاری از باکتری ها، قارچ ها و جلبک ها توانایی جذب و ذخیره فلزات سنگین از جمله مس را دارند. این فرآیند به دو صورت انجام می شود:
- جذب زیستی: در این حالت، یون های مس به سطح سلول های میکروارگانیسم ها متصل می شوند، بدون آنکه وارد سلول شوند. دیواره سلولی این موجودات معمولاً دارای گروه های عاملی مانند کربوکسیل، آمین، فسفات و هیدروکسیل است که با یون های مس پیوند یونی یا کووالانسی تشکیل می دهند.
- تجمع زیستی: در این حالت، فلز مس به داخل سلول نفوذ کرده و درون ساختارهای داخلی سلول ذخیره یا متابولیزه می شود. این مکانیسم معمولاً در میکروارگانیسم های زنده و فعال مشاهده می شود. از جمله میکروارگانیسم های مؤثر در این فرآیند می توان به گونه هایی از باکتری ها مانند Bacillus، Pseudomonas و Escherichia coli و نیز قارچ هایی چون Aspergillus و Penicillium اشاره کرد. بازده حذف مس در این روش بسته به نوع میکروارگانیسم، غلظت فلز و شرایط محیطی، بین 60 تا 95 درصد متغیر است.
استفاده از جلبک ها
جلبک های سبز، قهوه ای و آبی به دلیل سطح وسیع و حضور گروه های شیمیایی فعال، توانایی بالایی در جذب یون های فلزی دارند. در فرآیند فیكورمدییشن، جلبک ها از طریق جذب سطحی یا تجمع زیستی، فلزات سنگین را از آب حذف می کنند. گونه هایی مانند Chlorella vulgaris و Spirulina platensis از مؤثرترین جلبک ها در حذف مس محسوب می شوند.
جلبک ها می توانند یون های مس را به درون سلول خود جذب کرده و یا در سطح خارجی خود به صورت کمپلکس نگه دارند. علاوه بر حذف فلزات، آن ها باعث افزایش اکسیژن محلول در آب و بهبود کیفیت زیستی آن نیز می شوند. این روش بیشتر در تصفیه فاضلاب های صنعتی با غلظت کم فلزات سنگین و نیز در تصفیه پساب معادن کاربرد دارد. هزینه پایین، عملکرد پایدار و سازگاری زیست محیطی از مزایای آن است.
گیاه پالایی
گیاه پالایی یکی از مؤثرترین روش های طبیعی برای حذف فلزات از خاک و آب است. در این روش از گیاهان آبی یا خشکی دوست مقاوم به فلزات سنگین برای جذب، ذخیره یا تثبیت فلزات در بافت های گیاهی استفاده می شود. گیاهانی مانند نی، کنف هندی، تایفا و سنبل آبی توانایی بالایی در جذب مس از آب و فاضلاب دارند.
ریشه های این گیاهان یون های فلزی را جذب کرده و یا با ترشح ترکیبات آلی، شرایط شیمیایی محیط را برای رسوب فلزات مناسب می سازند. گیاه پالایی علاوه بر حذف فلزات، به کاهش BOD، COD و تثبیت لجن نیز کمک می کند. از این روش می توان در تالاب های مصنوعی یا سیستم های طبیعی برای تصفیه پساب های شهری و صنعتی استفاده کرد.
تالاب های مصنوعی و سیستم های اکولوژیکی
تالاب های مصنوعی یکی از کاربردی ترین فناوری های زیستی برای تصفیه فاضلاب های حاوی فلزات هستند. این سیستم ها شامل گیاهان آبزی، میکروارگانیسم ها و بسترهای فیلترکننده طبیعی (مانند ماسه و شن) هستند که به طور هماهنگ عمل می کنند. در این سیستم ها، فلزات سنگین از جمله مس از طریق مکانیسم های مختلفی مانند جذب سطحی روی بستر، جذب توسط ریشه گیاهان، رسوب گذاری بیولوژیکی و فعالیت میکروبی حذف می شوند.
تالاب های مصنوعی راندمان بالایی در حذف فلزات سنگین دارند و هزینه ساخت و نگهداری آن ها نسبت به روش های شیمیایی بسیار کمتر است. این روش ها بیشتر در تصفیه پساب های معدنی، فاضلاب شهری و صنایع کوچک به کار می روند و علاوه بر حذف مس، به بهبود کیفیت زیست محیطی مناطق اطراف نیز کمک می کنند.
ترسیب زیستی
در فرآیند ترسیب زیستی، میکروارگانیسم ها با ترشح ترکیباتی مانند سولفیدها یا فسفات ها باعث تشکیل رسوبات نامحلول از یون های فلزی می شوند. برای مثال، برخی از باکتری های بی هوازی قادرند از طریق احیای سولفات، یون سولفید تولید کنند. این یون ها با یون های مس واکنش داده و سولفید مس (CuS) نامحلول تشکیل می دهند که به راحتی ته نشین می شود.
این روش مشابه ترسیب شیمیایی با سولفیدها است، اما به جای مواد شیمیایی خطرناک، از فرآیندهای طبیعی و بیولوژیکی استفاده می شود. در نتیجه، زیست سازگارتر و ایمن تر است.

